Les
effets de l’alcool : I. L’alcool et le foie
- Approche
biologique : le métabolisme de la molécule d’éthanol
Comment
l’alcool est-il éliminé?
La
détoxication hépatique.
A
l’inverse des corps gras et du glucose, l’alcool ne peut être stocké.
Il est donc métabolisé. Il est ainsi principalement dégradé par les
cellules hépatiques (90%) mais également éliminé par sécrétion
directe (10%), c’est-à-dire par les reins (urine), les glandes
sudoripares (sueur) et les poumons (air expiré). La dégradation par le
foie est également appelée détoxication hépatique – elle est donc
la voie d’élimination la plus importante mais également la plus
lente (15mg.L-1.h-1) et la plus complexe :
l’éthanol, une fois absorbé subit une longue série de dégradations
pour aboutir à la molécule d’acétate.
La
détoxication hépatique commence avec l’oxydation de la molécule
d’éthanol en acétaldéhyde. Il y a 3 voies possibles :
·
l’alcool-déshydrogénase
·
le MEOS
·
la catalase
L’alcool-déshydrogénase
(ADH)
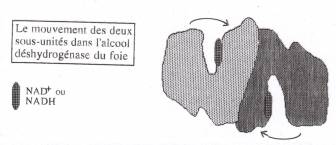 Cette
voie est celle qui est la plus utilisée, elle oxyde environ 75% de l'éthanol
absorbé. Avec l'aide d'une enzyme présente sur place, l'alcool-déshydrogénase,
un dimère de 2 chaînes identiques contenant chacune 374 Acides Aminés
associés à un ion zinc, ainsi qu'avec le cofacteur NAD+, s’effectue
la réaction d’oxydation de l’éthanol en acétaldéhyde : Cette
voie est celle qui est la plus utilisée, elle oxyde environ 75% de l'éthanol
absorbé. Avec l'aide d'une enzyme présente sur place, l'alcool-déshydrogénase,
un dimère de 2 chaînes identiques contenant chacune 374 Acides Aminés
associés à un ion zinc, ainsi qu'avec le cofacteur NAD+, s’effectue
la réaction d’oxydation de l’éthanol en acétaldéhyde :
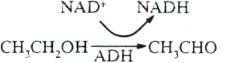
De
la même façon que la réoxydation des TH2 (transporteurs d'oxygène réduit)
libère de l'énergie dans la mitochondrie, la réoxydation du NAD+ en
NADH est exoénergétique et peut donc aboutir à une synthèse d'ATP.
Cependant, le système
n’est pas adaptable, c’est à dire qu’il ne peut accroître son
activité – en moyenne 1,6g d’éthanol par kilogramme de poids
corporel en 24h – soit 1,4L de vin pour un homme de 70kg.
Mais,
lorsque l'alcoolisation devient importante, l'activité de l'ADH diminue
au profit de l'oxydation par le MEOS.
Le
MEOS
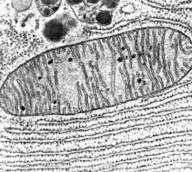 D'après
les scientifiques, cette voie ne serait réellement active que pour une
alcoolémie supérieure à 0,5 g/L. Le MEOS (Microsomal Ethanol
Oxidizing System) est principalement constitué du cytochrome P-450 et
de la NADH-cytochrome-c-réductase (enzyme). Il a une localisation
intramitochondriale (cf. ci-contre). Le cofacteur nécessaire à la réaction
est le NADPH : D'après
les scientifiques, cette voie ne serait réellement active que pour une
alcoolémie supérieure à 0,5 g/L. Le MEOS (Microsomal Ethanol
Oxidizing System) est principalement constitué du cytochrome P-450 et
de la NADH-cytochrome-c-réductase (enzyme). Il a une localisation
intramitochondriale (cf. ci-contre). Le cofacteur nécessaire à la réaction
est le NADPH :
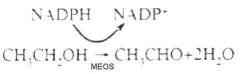
Contrairement
à la voie ADH, l'énergie produite ici n'est pas stockée sous forme
d'ATP mais dissipée sous forme de chaleur. C'est la raison pour
laquelle la valeur énergétique de l'éthanol est plus faible lorsqu'il
est consommé en grande quantité.
Chez
le sujet sain, le MEOS serait responsable de 25% de l’oxydation de
l’éthanol, d’où un « coefficient moyen d’éthyloxydation »
de 2g par kilogramme par poids corporel en 24h.
L'éthanol
provoque la prolifération du réticulum endoplasmique lisse microsomal
ce qui entraîne une augmentation de l'activité du P-450 lors
d'intoxications aiguës, ce qui a par exemple pour conséquence, la
rapidité de métabolisation des médicaments qui sont oxydés par le
MEOS chez un alcoolique.
Enfin,
si l'alcoolisation est vraiment trop forte (cas du buveur excessif et de
l’alcoolique chronique), c'est la voie d'oxydation par la catalase qui
intervient.
La catalase
La
voie de la catalase, ou xantine-catalase (XOC) est la plus nocive, elle
n'entre en jeu que lorsque les voies ADH et MEOS sont "saturées"
: par exemple lors d'intoxications alcooliques prolongées. La catalase
est une enzyme présente dans de nombreux tissus, mais surtout dans le
foie, les scientifiques la connaissent mal, d'ailleurs son rôle n'est
pas certain :
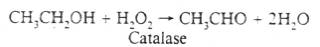
C'est
à ce moment que l'"alcool" est le plus dangereux : en effet
l'acétaldéhyde est un produit extrêmement toxique pour l'organisme :
30 fois plus que l'éthanol ! Il est ainsi à l'origine d'altérations
cellulaires, métaboliques et membranaires. D'ailleurs l'acétaldéhyde
peut s'associer avec d'autres protéines pour former des complexes
toxiques.
C'est
pour cette raison que l'organisme métabolise au plus vite cette molécule
en une autre : l'acétate.
Oxydation de
l’acétaldéhyde en acétate
La
réaction se fait en présence de l'enzyme Acétaldéhyde Déshydrogénase
qui est présente dans le cytosol (lorsqu'il y a peu d'acétaldéhyde à
dégrader, c'est l'enzyme mitochondriale qui intervient) :
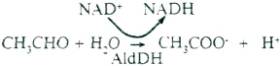
Une
fois formé, l'acétate va subir une dernière réaction qui produira de
l'acétyl CoA.
Catabolisme
de l’acétate
Cette
réaction se situe dans le cytosol des hépatocytes :
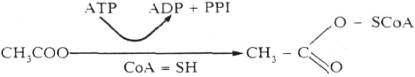
(CoA=SH=acétate thiokinase, enzyme)
Une
fois formé, l'acétyl CoA pourra :
- être
utilisé pour la synthèse des lipides
- former
de l'acétoacétate
- entrer
dans le cycle de Krebs et produire de l'énergie (7,4 kcal/g), du
CO2 et de l'eau
Le
cycle de Krebs
C’est une série de réactions métaboliques assurées par 7
enzymes pour décomposer totalement la molécule et produire de l'énergie,
de l'eau et du CO2 :

Schéma
récapitulatif :

B.
Pathologies hépatiques
liées à l’alcoolisme
Quels sont les effets de l’alcool sur le foie ?
Une
consommation chronique d'alcool entraîne des perturbations hépatiques
: la stéatose alcoolique, caractérisée par une surcharge lipidique,
qui peut évoluer vers une hépatite alcoolique, puis vers la cirrhose.
L'ensemble de ces lésions constitue les maladies alcooliques du foie.
Le risque de développer une cirrhose augmente avec la consommation
d'alcool, surtout à partir de 40 g par jour chez l'homme et de 20 g par
jour chez la femme. La femme serait ainsi plus vulnérable que l'homme
à l'alcool. La cirrhose peut entraîner des complications, notamment
des varices oesophagiennes et des hémorragies digestives.
Le
traitement des maladies hépatiques du foie repose essentiellement sur
l'abstinence, et une alimentation équilibrée.
Les
différentes études anatomiques montrent que seuls 6 % à 27 % des
patients alcooliques ont un foie normal ; 25 à 75 % d'entre eux présentent
une stéatose hépatique, 11 % à 30 % ont une hépatite, et 8 % à 30 %
développent une cirrhose.
La
stéatose
Elle
se caractérise par une surcharge lipidique. En dehors de l'alcool, il
existe d'autres causes de stéatose, comme l'obésité, le diabète,
.... L'hépatomégalie (augmentation anormale du volume du foie) liée
à l'alcoolisation peut s'expliquer par une surcharge en lipides dans 20
% à 30 % des cas, mais également par une surcharge en protides dans 20
% des cas, ou en eau dans 50 % des cas.
Hépatite
alcoolique
Les
cellules hépatiques présentent des lésions, augmentent de volume, se
nécrosent. Leurs parois s'épaississent. Certaines formes sévères
peuvent entraîner de la fièvre, des douleurs intenses, un ictère
(jaunisse), une polynucléose (augmentation du nombre des globules
blancs), une anémie, une élévation des immunoglobulines (anticorps),
plus rarement, un retentissement cérébral, et des anomalies de la
coagulation.
Cirrhose
Elle
se caractérise par un épaississement fibreux diffus. Les principales
complications souvent associées à la cirrhose :
- des
hémorragies digestives,
- un
ictère,
- des
infections : infection urinaire, septicémies, infections des
poumons, tuberculose pulmonaire, etc...
- une
surinfection par un virus de l'hépatite B ou C,
- un
cancer du foie.
Des
complications propres à l'intoxication alcoolique chronique sont également
souvent associées :
- cancer
des voies aéro-digestives supérieures,
- maladies
du système nerveux,
- pancréatite
chronique.
Il
existe cependant de nombreuses causes de cirrhose autre que l'alcool :
causes virales, biliaires, médicamenteuses, génétiques, métaboliques,....
Facteurs
de risque
Le risque de développer une cirrhose semble très variable selon
les individus. De façon générale, une consommation excessive d'alcool
pendant 10 à 20 ans est directement impliquée dans le développement
d'une cirrhose. Le risque de développer cette maladie augmente avec la
quantité quotidienne d'alcool consommée, notamment si elle est
comprise entre 40 et 160 g/jour.
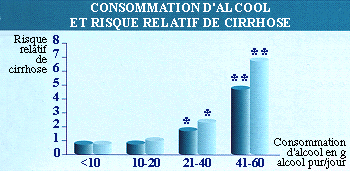 Pour
des quantités égales d'alcool, les femmes développent plus vite et
plus fréquemment une cirrhose. Cela peut s'expliquer par des différences
physiologiques (répartition du compartiment hydrique, enzyme ADH
gastrique, ...). Pour
des quantités égales d'alcool, les femmes développent plus vite et
plus fréquemment une cirrhose. Cela peut s'expliquer par des différences
physiologiques (répartition du compartiment hydrique, enzyme ADH
gastrique, ...).
|
![]()
![]()